Категории
Сменить пароль!
Сброс пароля!


Цель открытого исследования продолжительностью 16 недель состояла в оценке безопасности и фармакокинетики немолизумаба (нового моноклонального антитела, действующего на альфа-рецептор интерлейкина-31 (ИЛ-31)) у пациентов с атопическим дерматитом. Также анализировали наличие связи между концентрацией и клинической эффективностью немолизумаба (отношение фармакокинетики к фармакодинамике) и его влияние на уровни протеиновых биомаркеров.
Согласно полученным данным, терапия немолизумабом снижает уровень провоспалительных биомаркеров в коже. Это свидетельствует о том, что у подростков (в возрасте 12-17 лет) со среднетяжелым и тяжелым атопическим дерматитом цитокин регуляции нейроиммунного ответа ИЛ-31 является важным медиатором многих сигнальных путей.
Цель открытого исследования продолжительностью 16 недель состояла в оценке безопасности и фармакокинетики немолизумаба (нового моноклонального антитела, действующего на альфа-рецептор интерлейкина-31 (ИЛ-31)) у пациентов с атопическим дерматитом. Также анализировали наличие связи между концентрацией и клинической эффективностью немолизумаба (отношение фармакокинетики к фармакодинамике) и его влияние на уровни протеиновых биомаркеров.
В исследование были включены 20 пациентов с атопическим дерматитом, связанным с ним зудом и среднесуточной оценкой по числовой рейтинговой шкале максимального зуда (PP-NRS) не менее 4. Немолизумаб вводили подкожно в нагрузочной дозе 60 мг на исходном уровне, а затем в дозе 30 мг 1 раз в 4 недели до 12-й недели совместно с терапией местными ингибиторами кальциневрина или местными кортикостероидами. Период последующего наблюдения составил 8 недель. Для оценки уровня биомаркеров проводили сбор образцов рогового слоя эпидермиса и плазмы.
Фармакокинетика немолизумаба характеризовалась средним периодом полувыведения 16,7 ± 4,1 дня, линейной элиминацией и абсорбцией первого порядка. В течение периода лечения длительностью 16 недель минимальные значения концентрации находились в диапазоне от 2935 ± 1029 до 3292 ± 2018 нг/мл. У пациентов было отмечено статистически значимое улучшение сна, снижение интенсивности сыпи и зуда, а также снижение к 16-й неделе относительно исходного уровня индекса распространенности и тяжести экземы (EASI) и оценок по PP-NRS и числовой рейтинговой шкале оценки нарушений сна (см. таблицу 1).
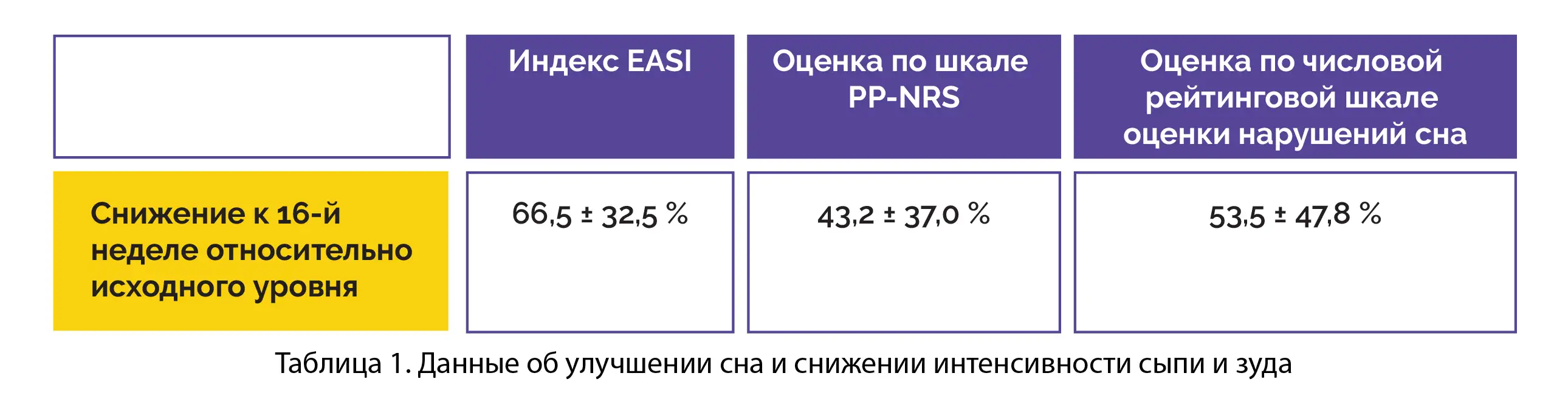
Согласно результатам оценки клинической эффективности, экспозиция и эффективность немолизумаба, определенные с помощью метода моделирования, у подростков и взрослых пациентов, получавших терапию по одинаковой схеме, были сопоставимы. Параметры фармакокинетики не зависели от возраста пациентов. Основным фактором, влияющим на фармакокинетику, была масса тела.
По результатам оценки образцов рогового слоя эпидермиса уровень связанных с атопическим дерматитом провоспалительных биомаркеров был ниже у пациентов с клиническим ответом на терапию немолизумабом (согласно данным о частоте достижения ответа EASI75 и оценки по шкале PP-NRS ≥4) и выше в пораженной коже (по сравнению с кожей без поражений).
У пациентов с ответом, определенным по индексу EASI, уровни 4 биомаркеров (VEGF, CCL27, CCL20, CCL22) были в 1,9-3,5 раза выше, чем у пациентов без ответа. Статистически значимой корреляции между клиническими показателями и уровнями биомаркеров в плазме не выявлено. Побочные эффекты отмечались у 33,3 % пациентов (n = 6) и были в основном средней или легкой степени тяжести.
Результаты оценки профилей безопасности и фармакокинетики немолизумаба у подростков с атопическим дерматитом соответствовали результатам, полученным в ходе предыдущих исследований немолизумаба у взрослых пациентов. Данные моделирования фармакокинетики/фармакодинамики, а также результаты общей оценки исследователем и оценки по шкале PP-NRS и индексу EASI у подростков в возрасте от 12 до 17 лет и взрослых пациентов свидетельствуют о сопоставимости профилей зависимости ответа от воздействия.
Dermatology and Therapy
Pharmacokinetics, Safety, Efficacy, and Biomarker Profiles During Nemolizumab Treatment of Atopic Dermatitis in Adolescents
Robert Sidbury и соавт.
Комментарии (0)